BENZATHIN BENZYLPENICILIN
Benzathinum benzylpenicillinum
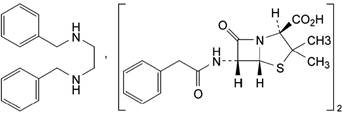
(C16H18N2O4S)2C16H20N2 P.t.l:
909,0
Benzathin
benzylpenicilin là phức hợp của (1:2) N,N’-dibenzylethan-1,2-diamin
với acid (2S,5R,6R)-3,3-dimethyl-7-oxo-6-[(phenylacetyl)amino]-4-thia-1-azabicyclo[3.2.0]heptan-2-carboxylic, phải chứa từ 96,0
đến 102,0% (C16H18N2O4S)2C16H20N2
và từ 24,0 đến 27,0% N,N’-dibenzylethylendiamin
(benzathin C16H20N2; p.t.l. 240,3) tính theo chế phẩm khan.
Chế phẩm có chứa hàm lượng nước
thay đổi và có thể chứa các tác nhân phân tán hoặc
tác nhân tạo hỗn dịch.
Tính
chất
Bột màu trắng.
Rất khó tan trong nước, dễ tan trong dimethylformamid và formamid, khó tan trong ethanol 96%.
Định
tính
Có thể chọn một trong hai nhóm định tính
sau:
Nhóm I: A
Nhóm II: B, C, D.
A. Phổ hồng ngoại (Phụ lục 4.2) của
chế phẩm phải phù hợp với phổ hồng
ngoại của benzathin
benzylpenicilin chuẩn (ĐC).
B. Tiến hành phương pháp sắc ký lớp
mỏng (Phụ lục 5.4).
Bản mỏng: Silica gel (TT)
đã được silan hóa.
Dung môi khai triển: Aceton - dung
dịch amoni acetat 15,4% (30 : 70), được điều
chỉnh pH đến 7,0 bằng amoniac (TT).
Dung dịch thử: Hòa tan 25 mg chế phẩm trong 5 ml methanol (TT).
Dung dịch đối
chiếu: Hòa tan 25 mg benzathin benzylpenicilin chuẩn (ĐC)
trong 5 ml methanol (TT).
Cách tiến hành: Chấm riêng biệt lên bản mỏng 1
µl các dung dịch trên. Triển khai sắc ký cho đến
khi dung môi đi được khoảng 15 cm. Làm khô bản
mỏng ngoài không khí, để bản mỏng trong hơi
iod đến khi các vết xuất hiện. Kiểm tra dưới
ánh sáng tự nhiên, hai vết chính trên sắc
ký đồ của dung dịch thử phải tương
ứng về vị trí, kích thước và màu sắc
với hai vết chính trên sắc ký đồ của dung
dịch đối chiếu. Phép thử chỉ có giá
trị khi trên sắc ký đồ của dung dịch
đối chiếu cho hai vết tách ra rõ ràng.
C. Cho khoảng 2 mg chế phẩm vào một ống
nghiệm có chiều dài 150 mm và đường kính 15 mm. Làm
ẩm với 0,05 ml nước và thêm 2 ml dung dịch formaldehyd trong acid sulfuric (TT). Lắc để
trộn đều, dung dịch không màu. Đặt ống
nghiệm vào trong cách thủy trong 1 phút, màu nâu đỏ xuất
hiện.
D. Thêm vào 0,1 g chế phẩm 2 ml dung dịch natri hydroxyd 1 M (TT), lắc đều
trong 2 phút. Lắc hỗn hợp trên hai lần, mỗi lần
với 3 ml ether (TT), lấy
lớp ether. Gộp các dịch ether, bay hơi đến khô
và hòa tan cắn trong 1 ml ethanol
50% (TT). Thêm 5 ml dung dịch acid picric (TT), đun
nóng ở 90 oC trong 5 phút và làm nguội từ từ.
Lọc lấy tinh thể thu được, kết tinh lại
trong ethanol 25% (TT) có chứa acid picric (TT) 1%. Nhiệt độ
nóng chảy của tinh thể thu được khoảng
214 oC (Phụ lục 6.7).
Giới hạn acid - kiềm
Cân 0,50 g chế phẩm, thêm 100 ml nước không có carbon dioxyd (TT) và lắc trong 5 phút.
Lọc qua phễu lọc xốp. Thêm vào 20 ml dịch lọc
0,1 ml dung dịch xanh bromothymol (TT).
Dung dịch có màu xanh lá hoặc vàng. Không được dùng
quá 0,2 ml dung dịch natri hydroxyd
0,02 M (CĐ) để chuyển màu của chỉ thị
sang màu xanh da trời.
Tạp chất liên quan
Tiến hành phương pháp sắc ký lỏng (Phụ lục 5.3).
Các dung dịch được chuẩn bị ngay trước khi dùng. Dùng máy lắc siêu âm để hòa tan mẫu thử (khoảng 2 phút), tránh để tăng nhiệt độ của mẫu thử.
Pha động A: Hỗn hợp dung dịch kali dihydrophosphat 3,4% đã được chỉnh pH đến 3,5 bằng acid phosphoric (TT) - methanol - nước (10 : 30 : 60).
Pha động B: Hỗn hợp dung dịch kali dihydrophosphat 3,4% đã được chỉnh pH đến 3,5 bằng acid phosphoric (TT) - nước - methanol (10 : 30 : 60).
Dung dịch thử: Hòa tan 70,0 mg chế phẩm trong 25 ml methanol (TT) và pha loãng thành 50,0 ml bằng dung dịch có chứa kali dihydrophosphat (TT) 0,68% và dinatri hydrophosphat (TT) 0,102%.
Dung dịch đối chiếu (1): Hòa tan 70,0 mg benzathin benzylpenicilin chuẩn (ĐC) trong 25 ml methanol (TT) và pha loãng thành 50,0 ml bằng dung dịch có chứa kali dihydrophosphat (TT) 0,68% và dinatri hydrophosphat (TT) 0,102%.
Dung dịch đối chiếu (2): Hút chính xác 1,0 ml dung dịch đối chiếu (1) cho vào bình định mức dung tích 100,0 ml; thêm pha động A vừa đủ tới vạch.
Điều kiện sắc ký:
Cột thép không gỉ (25 cm x 4,0 mm) được nhồi pha tĩnh là end-capped octadecylsilyl silica gel (5 mm).
Nhiệt độ cột: 40 oC.
Detector quang phổ tử ngoại đặt ở bước sóng 220 nm.
Tốc độ dòng: 1,0 ml/phút với chương trình dung môi:
|
Thời gian (phút) |
Pha động A (% tt/tt) |
Pha động B (% tt/tt) |
|
0 - 10 |
75 |
25 |
|
10 - 20 |
75 ® 0 |
25 ® 100 |
|
20 - 55 |
0 |
100 |
|
55 - 70 |
75 |
25 |
Thể tích tiêm: 20 ml.
Cách tiến hành:
Tiêm dung dịch thử, các dung dịch đối chiếu, ghi lại sắc ký đồ.
Xác định tính thích hợp của hệ thống bằng cách tiêm dung dịch đối chiếu (1).
Thời gian lưu tương đối so với benzylpenicilin của benzathin khoảng 0,3 đến 0,4 và của tạp chất C (acid benzylpeniciloic benzathid) khoảng 2,4. Điều chỉnh tỷ lệ methanol trong pha động nếu cần thiết.
Trên sắc ký đồ của dung dịch thử, diện tích của pic tương ứng với tạp chất C không được lớn hơn hai lần tổng diện tích hai pic chính trên sắc ký đồ dung dịch đối chiếu (2) (2,0%).
Bất kỳ pic phụ nào khác không được lớn hơn tổng diện tích hai pic chính của dung dịch đối chiếu (2) (1,0%).
Bỏ qua các pic có diện tích nhỏ hơn 0,05 lần tổng diện tích hai pic chính của dung dịch đối chiếu (2) (0,05%).
Nước
Từ 5,0 đến 8,0% (Phụ lục 10.3).
Dùng 0,300 g chế phẩm.
Độ vô khuẩn
Nếu chế phẩm dự định dùng để
sản xuất thuốc tiêm mà không tiến hành tiệt
khuẩn nữa thì phải đạt phép thử về độ
vô khuẩn (Phụ lục 13.7).
Nội
độc tố vi khuẩn
Lắc 20 mg chế phẩm
với 20 ml dung dịch natri
hydroxyd 0,1 N (TT) đã được pha loãng 1 thành 100,
lắc kỹ và ly tâm. Lấy dịch trong tiến hành
thử (Phụ lục 13.2, phương pháp E). Nội độc
tố vi khuẩn phải ít hơn 0,13 IU/ml. Nếu chế
phẩm dự định dùng để pha thuốc tiêm mà
không tiến hành các biện pháp loại nội độc
tố vi khuẩn thì phải đáp ứng yêu cầu này.
Định lượng
Phương pháp sắc ký lỏng (Phụ lục 5.3).
Các dung dịch thử, dung dịch
đối chiếu (1) và cột
sắc ký
giống như phần thử tạp chất liên quan.
Pha động: Hỗn hợp dung dịch đệm phosphat pH 3,5 - methanol - nước (
Detector quang phổ tử ngoại đặt ở bước sóng 220 nm.
Tốc độ dòng: 1,0 ml/phút.
Thể tích tiêm: 20 ml.
Cách tiến
hành:
Tiêm dung dịch thử, dung dịch đối chiếu (1).
Dựa vào diện tích
pic đáp ứng, tính toán hàm lượng của benzathin và
benzathin benzylpenicilin. Hàm lượng benzathin benzylpenicilin
bằng hàm lượng của benzylpenicilin nhân với
hệ số 1,36.
Bảo quản
Đựng trong
đồ bao gói kín.
Nếu là nguyên liệu vô
khuẩn: Đựng trong đồ bao gói kín, vô khuẩn và
tránh sự xâm nhập của vi khuẩn.
Nhãn
Phải quy định
rõ thời hạn sử dụng và điều kiện
bảo quản.
Ghi rõ tên và hàm lượng
của tác nhân phân tán hoặc tác nhân tạo hỗn dịch.
Ghi rõ nếu nguyên liệu
vô khuẩn hoặc không có nội độc tố vi khuẩn.
Loại thuốc
Kháng khuẩn.
Chế phẩm
Thuốc tiêm, viên nén và hỗn
dịch uống.